



食物为生命提供必需的营养物质,是细胞生长、发育、存活的关键。食物与免疫系统联系紧密。长期饥饿导致营养不良,会削弱免疫细胞的反应和执行能力,破坏黏膜屏障,使机体更易遭受病原侵袭。有趣的是,优质、足量的饮食对免疫系统同样弊大于利。工业化进程使得食物能够持续供应,但肥胖症、免疫力低下、自身免疫疾病的发病率反而居高不下。最新的研究表明,间歇禁食或短期饥饿有助于优化免疫系统、提高免疫力、降低疾病风险。然而,这种调控是高等动物在进化过程中独立获得的,还是代表了所有动物共同的生存策略,目前仍不清楚。
自然界中,野生动物的食物完全依赖觅食获得,并随季节变化而波动,使得饥饿司空见惯。鱼类、两栖类、爬行类等动物甚至进化出强大的耐受饥饿的能力。同时,它们也会主动减少摄食以应对病原感染或环境突变。低等脊椎动物的这些行为,为了解通过饮食干预优化免疫这一生存策略的进化,提供了理想模型。
近日,3200威尼斯vip杨嘉龙团队在国际权威期刊Cellular and Molecular Life Sciences上发表了题为Dietary restriction to optimize T cell immunity is an ancient survival strategy conserved in vertebrate evolution的研究论文,揭示了饥饿双向调控鱼类T细胞免疫的分子机制。

作者发现,T细胞是罗非鱼免疫系统响应饥饿的主要应答者。长期饥饿导致脾脏萎缩、T细胞凋亡和自发炎症,损伤了免疫细胞稳态,使鱼类更容易遭受细菌感染。相反,短期饥饿可在不影响免疫细胞稳态的前提下,提高T细胞应对抗原的激活和分化能力,增强抗感染免疫。

饥饿双向调控鱼类T细胞免疫
在机制上,饥饿诱发了T细胞自噬。而抑制自噬,则损伤了T细胞的激活、增殖和免疫功能。随着饥饿时间的延长,T细胞自噬加剧;长期饥饿触发强烈自噬,导致T细胞凋亡,破坏免疫细胞稳态。进一步的研究表明,饥饿通过生物能量枢纽AMPK通路介导T细胞的自噬。阻断AMPK通路,不仅降低了T细胞的自噬水平,造成免疫功能障碍,更损伤了T细胞在能量限制情况下维持存活的能力。实际上,细菌感染同样能够引发罗非鱼T细胞的自噬;而在短期饥饿的状态下遭遇感染,能够将自噬窗口提前,加快T细胞的应答速度,增强抗感染免疫能力,减少T细胞的凋亡,并降低组织损伤。
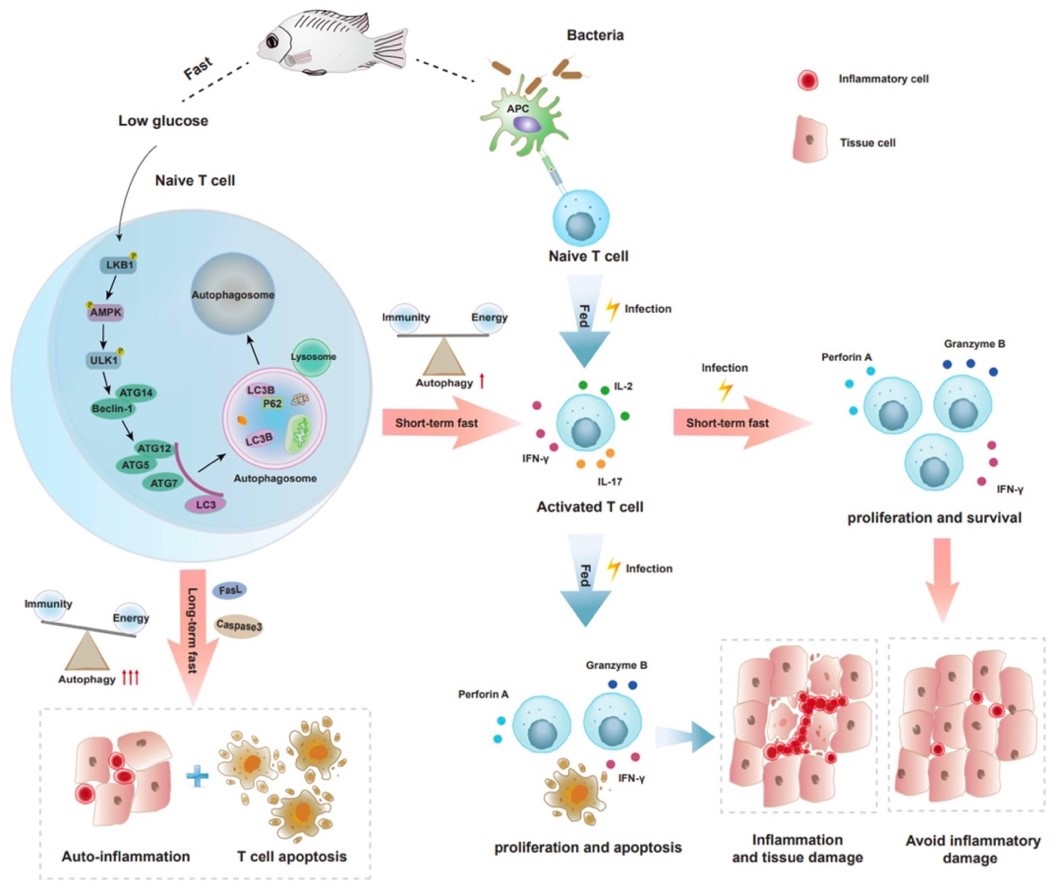
饥饿决定鱼类T细胞免疫的分子机制
综上所述,本研究阐明了饥饿双向决定鱼类T细胞稳态和免疫的机制。在食物充足、病原感染的情况下,鱼类主动停止摄食,通过短期饥饿触发轻度自噬,增强T细胞免疫,维持免疫和能量平衡,体现了免疫优先的原则。而在食物匮乏的情况下,长期饥饿迫使鱼类启动强烈自噬来回收能量,免疫系统也被牺牲,从而在最大程度上保障生命延续,体现了生存优先的原则。T细胞免疫与能量的权衡,代表了脊椎动物在长期的适应性进化中应对饥饿的生存策略。
3200威尼斯vip李坤明博士、韦秀梅副教授、李康博士生为该论文的共同第一作者,杨嘉龙教授为本文通讯作者。该研究受到国家自然科学基金优秀青年科学基金项目、面上项目等资助。

杨嘉龙教授(左)、李坤明博士(右)
原文链接:https://link.springer.com/article/10.1007/s00018-023-04865-x